비중격 외비성형술에서 이식 재료로써 Polylactic-Co-Glycolic Acid Plate의 유용성
Efficacy of Polylactic-Co-Glycolic Acid Plate as a Graft Material in Septorhinoplasty
Article information
Trans Abstract
Background and Objectives
Polylactic-co-glycolic acid (PLGA) plate has been recognized for its biocompatibility and biomechanical properties and used widely in various clinical fields. The aim of this study was to evaluate the usefulness and reliability of PLGA plate as a graft material in septorhinoplasty.
Subjects and Method
Medical records were retrospectively analyzed for patients who underwent septorhinoplasty including extracorporeal septoplasty from January 2017 to June 2020. We evaluated demographics, diagnosis, operation techniques, and complications of PLGA plate as a graft material used in these patients.
Results
A total of 33 patients were enrolled in this study. Twenty-eight were male and 5 were female. The median age was 32 years old. The follow-up period after surgery was 6-32 months, and the mean follow-up period was 18.03 months. The PLGA plate was used in unilateral spreader graft (n=17), bilateral spreader graft (n=10), batten graft (n=3), strengthening of septal extension graft (n=2) and columellar strut graft (n=3), and fixing L-strut during extracorporeal septoplasty (n=12). During the follow-up period, no patient experienced extrusion or exposure of the grafts. Mild complications, such as redness of the columella skin, granulation in the marginal incision site, and pain on the nasal dorsum were observed in three patients; these complications were temporary and patients improved with conservative treatments.
Conclusion
The PLGA plate may be a useful graft material in correcting deviated nose especially when the harvested septal cartilage is insufficient and if used carefully in limited locations such as L-strut and columella.
서 론
사비에 동반된 비중격 만곡증을 교정하기 위한 비중격 교정술을 시행할 때 비주절개를 통한 개방비성형접근법은 비배부와 비중격에 대한 넓은 시야를 제공하여 동반된 변형을 교정하는 데 장점이 있다[1]. 개방비성형접근법을 통한 비중격 외비성형술 및 비중격 체외교정술(extracorporeal septoplasty) 시 비배부의 변형된 비중격 교정은 필수이며, 이때 주로 비중격에서 채취한 연골은 가장 이상적인 이식 재료로써 펼침이식(spreader graft), 버팀목이식(batten graft), 비중격 연장이식(septal extension graft) 등의 술기에 이용된다[2-5]. 하지만 사비환자의 경우 비골 및 비중격 골절 등의 외상 과거력이 있는 경우가 대부분이고, 비중격 연골의 골화 및 심각한 변형이 동반된 경우가 흔해서 이식 재료로써 사용하기에 양이 충분하지 않은 경우가 있다. 이 경우 비배부 비중격 변형을 교정하기 위해 이개연골이나 늑연골을 이용한 자가이식(autologous graft) 혹은 이물이식(allograft)을 고려해야 한다[6-8]. 하지만 자가 늑연골이나 귀연골을 이용하는 경우는 침습적이고, 수술 이후 공여부에 흉터, 혈종, 기흉 등의 부작용이 발생할 수 있으며, 골화가 진행된 경우 충분한 양의 연골을 얻을 수 없다는 단점이 있다[9]. 따라서, 이를 대체하기 위하여 polydioxanone (PDS), porous high-density polyethylene (pHDPE; MedporⓇ; Stryker, Kalamazoo, MI, US), polylactic acid (PLA), polylactic-co-glycolic acid (PLGA) 등의 이물이식 재료들이 소개되어 왔다[9-12].
이들 재료 중 PLGA는 PLA와 poly-glycolic acid(PGA)로 이루어진 고분자로써 생체적 합성과 생체 역학적 특성을 인정받아 임상적으로 다양한 분야에서 활용되고 있다[13]. PLGA plate는 단단한 재질이지만 두께가 비교적 얇아서 돌출의 염려가 없고, 가공하기가 쉬우며, 채 모양의 구멍들이 있어서 연골에 봉합하기 쉽기 때문에 비성형술 시 다방면에서 활용도가 높다. 본 연구에서는 외비성형술에서 PLGA plate를 이식 재료로 사용하였을 때 이물이식 재료로써 유용성과 안전성에 대하여 알아보고, 다른 이물이식물과 비교하였을 경우의 장단점을 문헌 고찰을 통해 살펴보고자 한다.
대상 및 방법
2017년 1월-2020년 6월까지 충남대학교병원 이비인후과에 입원하여 비중격 외비성형술 및 비중격 체외교정술을 받은 환자들 중 PLGA plate를 수술 중 사용하였던 환자들을 대상으로 의무기록을 후향적으로 분석하였다. 총 112명의 환자 중 33명의 환자에서 PLGA plate를 사용하였고, 이 환자들의 의무기록을 분석하여 성별, 나이, 진단명, 수술기록지의 수술 방법, 추적 관찰 기간, 합병증 등을 조사하였다. 본 연구는 해당 기관 임상연구심의위원회의 승인(IRB FILE No. 2020-12-087)하에 진행되었다.
수술 방법
모든 수술은 숙련된 1인의 술자가 전신마취하에 개방접근법으로 진행하였다. 비중격 외비성형술은 비중격연골의 L형 지주를 보존하면서 비중격연골을 채취하고 만곡된 비중격골부를 제거하여 비중격 교정술을 시행하였다. 비중격 체외교정술인 경우 비중격의 재건을 위해 L형 지주 중 두부의 일부분을 남겨둔 채 나머지 연골부와 골부를 모두 제거하였다. 비중격의 교정을 위해 버팀목이식, 펼침이식, 비중격 연장이식, swing door technique, figure of 8 suture 등의 술기를 적용하였는데, 채취한 비중격연골이 골화 또는 비틀림으로 인해 양이 충분하지 않을 경우 PLGA plate (Biobsorb αⓇ, 29×25.2×0.3 mm; OSTEONIC Co., Ltd., Seoul, South Korea) (Fig. 1A)를 이용하여 서로 다른 이식술을 시행하였다. 필요에 따라 비골절골술, 비첨이식, 비배부융비술 등을 추가적으로 시행하였다.

Extracorporeal septoplasty using PLGA plate. A: The shape and size of PLGA plate was shown. B: The harvested septal cartilage was insufficient to use as a graft material in extracorporeal septoplasty. C: L-strut was reconstructed using septal cartilage and a PLGA plate. D and E: Schematic drawings of septal reconstruction using septal cartilage and a PLGA plate. F: Patient’s photo taken preoperatively and postoperatively at 5 months. PLGA, polylactic-co-glycolic acid.
L형 지주 강화
비중격 체외교정술 시 채취한 비중격연골이 부족한 경우, 새로 재단하여 만든 비중격연골(L형 지주의 미부)과 남겨진 비중격연골 두부(L형 지주의 상단부)를 결합할 때 PLGA plate를 이용하였다(Fig. 1). 채취한 비중격연골의 양에 따라 PLGA plate를 일측 또는 양측에 사용하여 5-0 PDSⓇII (ETHICON, Cornelia, GA, US)로 여러 차례 봉합하여 비중격연골을 안정화시켰다. 비중격미부는 전비극 부위의 골막에 3-0 coated VICRYLⓇ (ETHICON, Cornelia, GA, US)로 봉합하였다.
펼침이식, 버팀목이식
비중격연골 비배부의 만곡이나 변형이 관찰된 경우 채취한 비중격연골의 양에 따라 일측 또는 양측에 PLGA plate를 이용하여 펼침이식을 시행하였다(Fig. 2). 비중격연골을 채취하고 남은 L형 지주 부위의 만곡이 심한 경우 펼침이식과 별도로 PLGA plate를 이용하여 버팀목이식을 일측 또는 양측에 시행하였다(Fig. 3A).
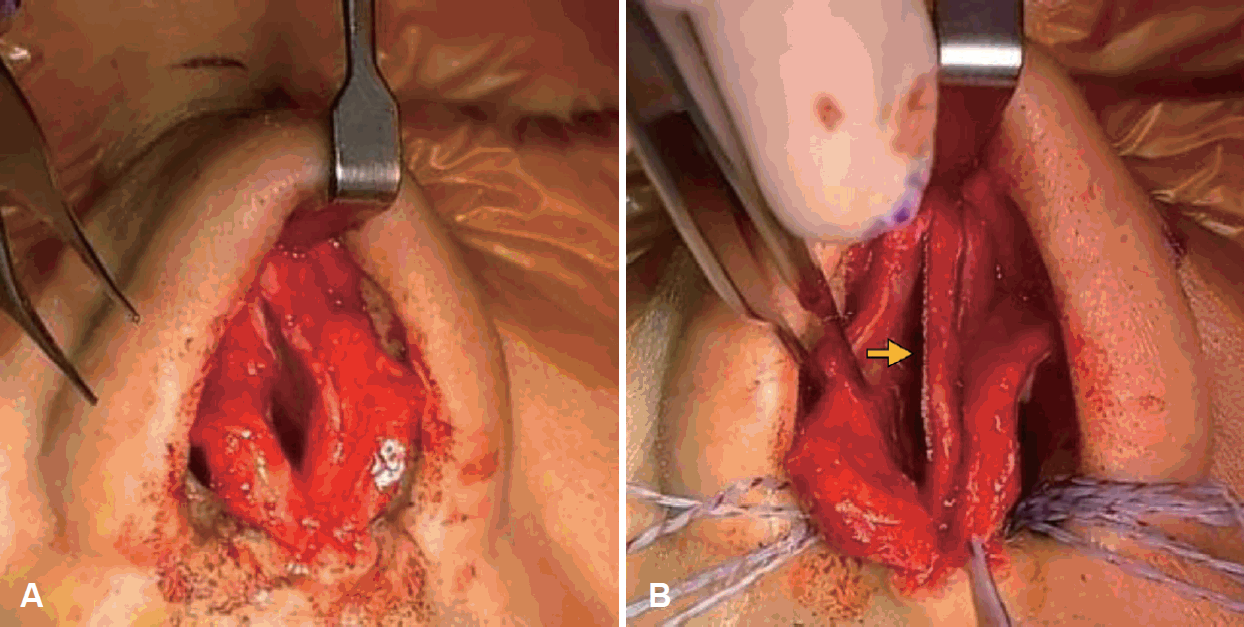
Correction of dorsal septal deformity using PLGA plate. A: Intraoperative photo shows dorsal deformity of nasal septum. B: A unilateral spreader graft was applied using a PLGA plate, and septal deviation is corrected. The arrow points to the PLGA plate. PLGA, polylactic-co-glycolic acid.

Pictures during surgery using PLGA plate. A: PLGA plate was used as a batten graft on one side of the L-strut. B: The septal cartilage wrapped around the PLGA plate on both sides to create a columellar strut graft. And the graft was transplanted into the columellar. The arrows point to the PLGA plate. PLGA, polylactic-co-glycolic acid.
비주지주이식, 비중격 연장이식
비주지주이식(columella strut graft)의 경우 하외측비연골의 내측각이 변형되었거나 연골 자체의 강도가 약하여 비첨의 지지가 약할 것으로 예상되는 경우, 혹은 추가적인 비첨 이식을 위한 비첨 지지가 필요한 경우에 시행하였다. 비주지주이식을 위한 충분한 양의 비중격연골이 없는 경우에만 PLGA plate를 제한적으로 사용하였는데, 이개연골을 이용한 비주지주이식을 할 경우와 채취한 비중격연골 중 곧은 부분이 없는 경우 PLGA plate를 두 개의 연골 사이에 끼워 넣고 봉합하여 노출이 안 되도록 주의하면서 비주지주이식을 강화하였다(Fig. 3B).
비중격 연장이식에 쓰인 비중격연골이 약하여 충분히 비첨을 지지하지 못할 것으로 생각되는 경우 PLGA plate를 비중격연장이식 연골에 덧대어 이식을 강화하였다. 이 때 PLGA plate는 비중격 연장이식보다 크기가 작게 디자인하여 돌출되지 않게 하였다.
결 과
총 33명의 환자가 연구에 포함되었고, 남성이 28명(84.8%), 여성은 5명(15.2%)이었다. 연령 분포는 18-76세였으며, 평균 연령(median age)은 32세였다. 비중격 외비성형술을 받은 환자는 21명(63.6%), 비중격 체외교정술을 받은 환자는 12명(36.4%)이었으며 비내접근술을 이용한 환자는 없었다. 각각의 환자에 대한 진단은 비중격 만곡증이 20명, 비중격 만곡증과 사비로 진단받은 환자가 13명이었고, 비중격 외비성형술을 받은 환자 중 한 명의 환자는 8개월 전 수술 이후 재수술을 한 환자였다. 수술 이후 외래 경과 관찰 기간은 6-32개월, 평균 추적 관찰 기간은 18.03개월이었다(Table 1).
수술 중 다양한 이식편(graft)을 시행하기 위한 비중격연골의 양이 부족한 경우 PLGA plate를 비중격연골 대신 사용하였다. PLGA plate 이식방법은 비중격 체외교정술 시 L형 지주를 고정하기 위해 사용한 경우가 12명, 일측 펼침이식 17명, 양측 펼침이식 10명, 버팀목이식이 3명, 비중격 연장이식을 위한 지지 2명, 비주지주이식의 지지 3명이었다(Table 2).
수술 후 모든 환자에 대해 주기적으로 비내시경을 포함한 신체검사를 하였으며, 추적 관찰 기간 중 PLGA plate 이식물의 돌출 및 노출이 발생한 환자는 없었다. 추적 관찰 기간 중 일측 펼침이식을 시행한 환자 중 1명에서 술후 2주째에 비주에 발적이 발생하였고, 양측 펼침이식을 시행한 환자 중 1명에서 술후 4주째에 좌측 비익 경계절개선 부위에 육아종이 발생하였으나 항생제와 보존적 치료로 호전되어 경과 관찰하였다. 양측 펼침이식과 버팀목이식을 같이 시행했던 1명의 환자가 술후 4주째에 비배부 통증을 호소하였는데, 진통제를 1주일간 복용 후 통증이 조절되었다(Table 3).
고 찰
비중격 외비성형술 또는 비중격 체외교정술에서 변형된 L형 지주를 효과적으로 교정하고, 비배부를 반듯하게 하며, 내비 밸브의 기능적 개선을 목적으로 채취한 비중격연골을 이용하여 펼침이식이나 상외측비연골을 이용한 자가펼침이식(autospreader graft)을 시행하게 된다[14]. 그러나, 이전에 받은 외상으로 인한 비중격연골의 골화나 변형으로 자가 비중격연골을 충분히 얻지 못하는 경우 비중격 이외의 연골을 채취하여야 한다. 하지만 자가연골이식으로 많이 사용하는 이개연골이나 늑연골은 채취하는데 추가로 시간이 더 소요되고 공여부의 합병증 발생의 가능성이 있는 단점이 존재한다. 이러한 이유로 최근 이물이식의 필요성이 점차 증가하고 있다[15].
이물이식의 재료 중 expanded polytetrafluoroethylene, pHDPE, silicone 등의 재료는 주변 조직으로 흡수되지 않고 분해되지 않아 migration, extrusion, 이물반응으로 인한 감염 등의 위험성이 있다[16]. 따라서, 비흡수성을 대신하여 흡수성 이물이식 재료가 소개되어 왔는데, polycaprolactone (PCL)은 낮은 온도에서도 잘 녹는 특성과 생체 적합성을 인정받아 3D printing 기술을 이용한 두개안면부 재건이나 약물전달체 재료로써 각광을 받고 있다[17].
그러나 PCL plate (OsteomeshTM; 39×25×1.25 mm; Osteopore, Singapore)는 1.25 mm로 본 연구에 사용된 0.3 mm의 PLGA plate에 비해 두께가 두꺼워 체내 가수 분해 속도가 24개월 이상 필요하며 체내에서 이산화탄소와 물로 가수분해되지만 주변 pH에 영향을 줄 수 있다[18]. 따라서 분해 속도에 따른 돌출, 감염 등의 합병증 발생이 높을 수 있고, Kim과 Choi [17]에 의하면 수술 직후 환자가 강직성(stiffness)을 호소할 수 있다는 단점이 있다. 또한 PCL plate의 급여 수가가 379730원인 반면 PLGA plate는 비급여 수가 196000원으로 비용적인 측면에서도 효율적이다.
Crystalline polymer인 PDS의 경우 구멍(perforation)이 있는 0.15 mm plate와 구멍이 없는 0.25 mm plate로 구분되는데, 얇은 plate는 frame를 지지할 수 있는 강도가 부족하기 때문에 두꺼운 0.25 mm plate를 주로 사용하게 된다[19]. PDS는 체내에서 8개월 이내에 분해되어 흡수되지만, 0.25 mm plate는 사용시 바늘을 이용하여 구멍을 만들어야 하는 불편함이 있고 점막연골막피판(mucoperichondrial flap)으로의 적절하지 못한 혈류 공급으로 인해 saddle nose와 같은 합병증 발생 빈도가 더 높아질 수 있다는 보고가 있다[8,20].
PLGA는 폴리에스터 계열로 PGA와 PLA의 합성 고분자이며, 친수성인 glycolic acid와 소수성인 lactic acid 사이의 에스터결합 붕괴로 결국 물과 이산화탄소로 가수분해된다[21]. PLGA는 PGA와 PLA의 혼합 비율에 따라 분해 속도가 조절되지만 일반적으로 6개월 이내에 분해되는 것으로 알려져 있다[22]. 본 연구에서 환자들의 수술 후 외래 추적 관찰 기간은 6-32개월이었으며, 이는 PLGA plate가 생체 내에서 분해되기에 충분한 시간으로 생각할 수 있고, 추적 관찰 기간 동안 감염이나 염증과 같은 주요 합병증은 발생하지 않았다. 3명의 환자가 비주의 발적, 절개선의 육아조직 생성과 비배부 통증이 각각 발생하였는데, 모두 수술 후 4주 이내에 발생하였으므로 PLGA plate의 분해과정에서 생기는 염증 반응과의 관련성은 없다고 볼 수 있으며 모두 보전적인 치료로 호전되었다. 생체에 무해한 물과 이산화탄소로 분해가 되기 때문에 PLGA plate는 생체 안정성이 보장되고, 이물반응 발생 가능성이 상대적으로 낮은 것으로 알려져 있다[15,23]. 또한, 본 연구에 사용된 PLGA plate는 구멍이 있기 때문에 수술 중 술자가 구멍을 만들지 않아도 되는 이점이 있고 얇은 두께에 비해 재질이 단단하여 적절한 기계적 강도를 제공할 수 있어서, 일측 펼침이식, 양측 펼침이식, 비중격 연장이식, 비주지주이식, 버팀목이식 등 서로 다른 위치에서도 이식물의 돌출 위험을 줄이면서 유용하게 응용될 수 있다는 가능성을 확인할 수 있었다.
PLGA는 체내에서 분해되며 PCL과 비슷하게 연골 형성을 일으키며[24] 분해 과정 중 주변 조직의 pH를 국소적으로 감소시키면서 염증 반응을 일으키며 흡수되고, 따라서 주변 조직의 상처 치유에 영향을 줄 수 있다[25]. 본 연구의 환자들은 감염 또는 염증반응에 의한 구축 등 심각한 부작용은 발생하지 않았지만 눈에 띄지 않는 염증반응으로 인해 외형적 변화가 서서히 진행될 가능성은 있다. 따라서, 향후 1년 이상의 장기간의 추적 관찰을 통하여 코 높이의 변화나 코 모양의 변형과 같은 상처치유 과정에서 보일 수 있는 변화를 장기간에 걸쳐 관찰할 필요가 있다. 또한, 조직치유 과정에 영향을 미칠 수 있으므로 비첨 부위나 비주 부위처럼 혈류의 공급에 민감하고 피부가 얇은 부위에 PLGA plate를 사용할 때는 각별한 주의를 기울여야한다.
결론적으로 PLGA plate는 비중격연골의 심한 변형이나 골화로 채취한 비중격연골의 양이 충분하지 않을 경우 비중격이나 비주 등 제한적인 위치에 신중하게 사용한다면, 비중격 외비성형술 및 비중격 체외교정술 시 안전하고 유용한 이식 재료로 사용될 수 있을 것이라 생각한다.
Acknowledgements
I would like to thank colleagues of our institute for support of time to finish the research. I would also like to thank the patients who provided photos for this study for the advancement of septorhinoplasty.
Notes
Author Contribution
Conceptualization: Yong Min Kim, Soo Kyoung Park, Ki-Sang Rha. Data curation: Min-Su Kim, Se Yeon Im. Formal analysis: Ki-Sang Rha. Resources: Soo Kyoung Park. Supervision: Ki-Sang Rha. Writing—original draft: Jae-Yoon Kang. Writing—review & editing: Jae-Yoon Kang, Yong Min Kim.