서 론
두경부암은 전 세계에서 매년 40만 명에서 60만 명 정도가 새로이 발생하고, 30만 명 가까이 사망하는 6번째로 흔한 암이다[1]. 30~40%의 환자들은 초기 단계에서 진단이 되어 70~90%의 5년 생존율을 보이나, 나머지의 환자들은 진행된 단계에서 진단이 되며 적절한 치료에도 불구하고 생존율은 30~ 40%로 떨어지게 된다[2,3]. 구강, 인두, 후두, 경부 등 다양한 부위에서 발생하는 두경부암의 특성상 부위에 따른 차이는 있겠지만 림프절 전이는 모든 두경부암의 치료 성적에 가장 큰 영향을 미치는 예후 인자이다. 림프절 전이가 있는 경우에는 그렇지 않은 경우에 비해 예후가 절반으로 감소하며, 특히 피막 외 침범이 있는 림프절 전이가 있으면 생존율이 10~25%까지 떨어지게 된다[3-6]. 또한 경부 림프절 전이는 향후 경부 이외 부위로의 원격전이의 발판이 될 수도 있다[7].
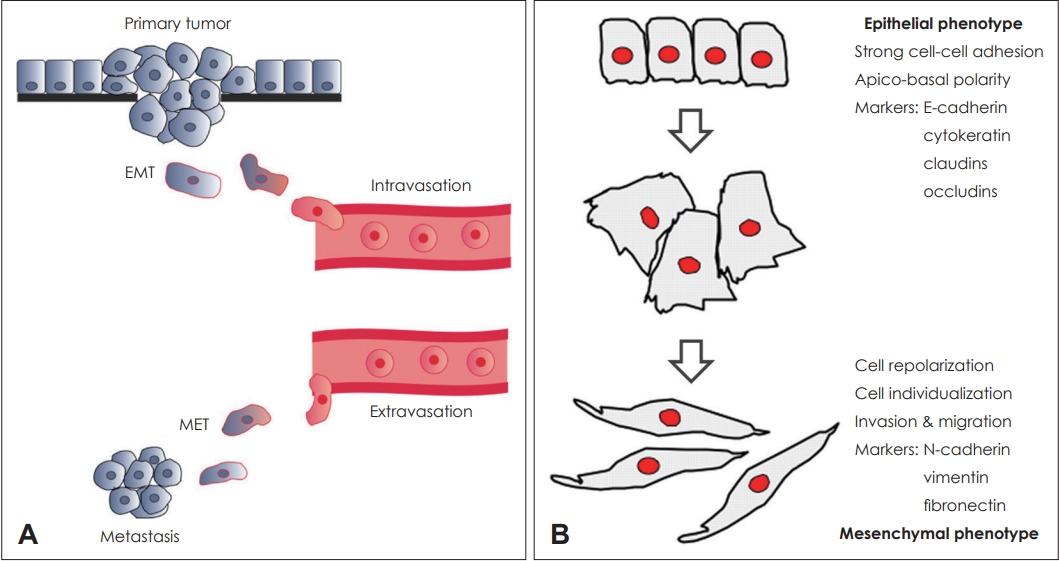
암세포가 림프관을 타고 전이를 하기 위해서는 세포의 이동이 필요하다. 암세포가 이동하기 위해서는 원발 부위에서 떨어져 나와서 기질로 침습하여 혈관이나 림프관에 들어가야 한다. 안정적으로 세포군락을 이루던 상태에서 다른 세포와 떨어져 이동을 하기 위해서는 세포의 특성들이 바뀌어야 하는데 이러한 과정을 상피-간엽이행(epithelial-mesenchymal transition, EMT)이라 한다[8-10]. 상피세포는 정방형 모양으로 위쪽과 기저쪽이 확실히 구분되는 극성을 띄며 세포간 접촉을 유지하려는 특성을 가지고 있다. 이에 반해 간엽세포는 세포의 모양이 섬유아세포형으로 극성이 사라지고 다른 세포와의 접촉 없이 이동과 침윤이 용이하게 된다. 상피-간엽이행은 안정적인 세포간 결합을 이루고 있던 상피형 세포가 이동에 편한 간엽형 세포로 변화하는 복잡하고 가역적인 과정으로 종양의 생성, 악성화 과정, 암줄기세포, 암세포의 이동, 전이, 치료에 대한 저항성 등 암세포의 다양한 과정에 모두 연관되어 있는 것으로 알려져 있다(Fig. 1) [11-15]. 두경부종양에서도 다른 기관의 암에 비해서는 부족하지만 상피-간엽이행과 관련된 연구들이 진행되고 있다[16,17]. 하지만 두경부암을 포함한 대부분의 연구들은 상피-간엽이행이 일어나기 전과 후의 상태를 나타내는 표지자들의 발현량을 비교하는 것이 주를 이루며, 암세포에서 상피-간엽이행이 일어나는 과정에 대한 연구는 아직 미비한 상태이다. 암의 진행과 전이에 대한 이해 및 추후 치료적 접근을 위해서는 암세포에서 일어나는 상피-간엽이행의 과정에 대한 명확한 이해가 필수적이다.
이번 종설에서는 암세포에서 상피-간엽이행이 일어나는 과정 중에 세포 내에서 일어나는 변화들에 대해 현재까지 알려진 내용들을 중심으로 알아보고 두경부암에서 상피-간엽이행과 관련된 임상연구들을 간단히 살펴보고자 한다.
상피-간엽이행과 카데린
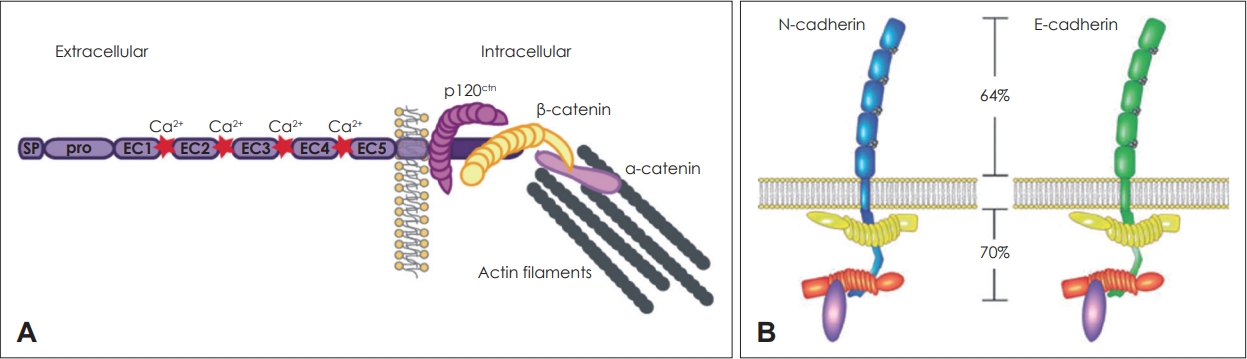
상피세포들의 세포간 결합 중 부착연접(adhering junction)에는 카데린(cadherin)이라는 세포부착분자(adhesion molecule)가 인접한 두 세포를 연결해 준다[18]. 카데린은 세포막을 관통하여 위치하는 수용체 단백질로 5개의 세포외구역(extracellular domain)을 가지며, 인접세포에 위치한 다른 카데린과 결합하여 세포간의 단단한 결합의 유지시킨다. 카데린의 세포내구역(intracellular domain)은 α-, β-카테닌과 결합하여 세포의 전반적인 골격을 형성하는 액틴과 연결된다. 카데린에 의한 세포간 결합은 세포군락을 이루기 위해 필수적이며 부착연접 뿐아니라 밀착연접(tight junction)과 같은 다른 세포결합의 형성과 붕괴에도 영향을 미치게 된다. 또한 세포 내외를 관통하는 구조적인 특성상 인근세포로부터 전해지는 물리화학적인 신호를 세포 내로 전달하기도 한다. 카데린의 종류는 100여 가지 이상이 있으나 가장 기본적으로 E-카데린과 N-카데린이 있으며 이 둘은 구조적으로 매우 비슷하다[19]. 둘 다 세포간 결합에 의해 전달되는 물리적 힘의 정도에 따라 세포외구역의 형태가 달라지고 이는 화학적 신호로 변환되어 세포 내에 전달된다. E-카데린은 대부분의 정상적인 상피세포에서 발현된다. N-카데린은 세포의 이동이 비교적 활발한 신경세포나 간엽세포들에서 잘 발현된다. 단백질의 골격도 비슷하고 세포막에서의 역할도 비슷하지만 암세포에서는 그 기능이 극명하게 차이가 난다(Fig. 2) [20,21].
암세포가 안정적으로 세포간의 접촉을 잘 이루고 있을때는 세포막에 E-카데린이 주로 존재한다. E-카데린은 주변 세포의 E-카데린과 연결되여 안정된 결합 상태를 만들고 세포를 상피표현형으로 유지시킨다. 세포간 결합 부위에 외부로부터의 물리화학적인 자극이 발생하면 상피-간엽이행이 시작되고 세포간 접촉부위의 수용체 단백질들의 분포가 변화하기 시작한다. 제일 먼저 시작되는 변화는 여러가지 경로를 통해 기존에 세포막에 존재하던 E-카데린들이 분해되고 새로 만들어지지 않는 것이다. E-카데린이 감소하게 되는 과정은 크게 전사조절(transcriptional control)과 그 후 과정으로 나눌 수 있다. 상피-간엽이행이 시작하게 되면 Snail, Slug, ZEB1, ZEB2, E47, Twist 등의 다양한 전사인자들이 TGF-β, HGF, EGF, Wnt, Notch 등의 경로를 통해 핵내에서 E-카데린의 전사를 억제하게 된다. 이처럼 핵 내부에서 새로운 E-카데린의 생성을 억제하는 동안 세포막에서는 기존에 만들어져 세포간 결합을 이루고 있는 E-카데린의 붕괴가 동시에 진행된다. 상피-간엽이행이 시작되면 Src나 FAK 등에 의해 E-카데린의 세포내구역이 인산화되게 되고, 이어서 주변에 있던 E3-ubiquitin-ligase Hakai, γ-secretase 등에 의해 붕괴되어 정상적인 기능을 소실하게 된다. E-카데린에 붙어있던 β-카테닌도 인산화되면서 E-카데린과 떨어진 후 일부는 핵내부로 진입하여 E-카데린의 생성을 억제하게 된다.
한편 E-카데린에는 액틴과 연결시켜주는 α-, β-카테닌 외에 p120-카테닌도 연결되어 있다. P120-카테닌은 액틴의 재합성 과정을 조절하여 세포의 형태를 바꾸고 세포 이동에 중요한 역할을 하는 Roh GTPase의 활성화를 조절하여 카데린-카테닌-액틴 조합을 안정화하는 역할을 한다. E-카데린의 세포내구역에 p120-카테닌이 안정적으로 붙어있을 때는 E-카데린의 기능이 정상적으로 유지되지만, E-카데린에서 p120-카테닌이 떨어져 나오게 되면 E-카데린을 중심으로하는 카테닌-액틴 연결이 끊어지게 된다.
카데린 전환(Cadherin Switching)
부착연접에서 큰 비중을 차지하며 세포간 연결에 중요한 역할을 하던 E-카데린이 감소하게 된 후 발생하는 세포막의 빈 공간은 N-카데린으로 채워지게 된다. E-카데린과 구조적으로 거의 비슷한 형태를 가진 N-카데린은 부착연접 내 맞은편 세포에 있는 N-카데린과 결합하고 세포 내부에서는 α-, β-카테닌을 통해 액틴과 연결되어 있다. E-카데린에서 떨어져 나와 세포질에 떠돌던 P120-카테닌 역시 N-카데린과 결합하여 N-카데린을 중심으로하는 카테닌-액틴 연결을 더욱 공고하게 유지시키게 된다. 이러한 경로를 통해 안정적인 상태의 세포막 주로 분포하던 E-카데린이 감소하고 그 자리에 N-카데린이 증가하게 되는 과정을 카데린 전환(cadherin switching)이라 한다. 카데린 전환은 상피-간엽이행 과정 중 가장 특징적이며 중요한 변화이다[18,22].
RhoA, Rac1, Cdc42는 Ras-related GTP-binding protein으로 세포 외부로부터의 자극에 대한 반응으로 액틴에 의한 세포골격의 합성과 분해를 조절하는 역할을 한다. 상피-간엽이행이 일어나는 동안 액틴의 재배열을 조절하여 세포의 모양을 변형시키고 세포이동이 일어날 수 있도록 한다. RohA는 actin stress fiber를 강화시켜서 세포간 결합을 안정화한다. 이에 반해 Cdc42와 Rac1은 branch-like actin protrusion을 만들어 세포의 무게중심을 이동시켜 세포간 결합을 약화시키며 특히 Rac1은 RhoA에 대해 길항적으로 작용한다. 세포막 주변에 RhoA가 활성화되어 있는 상태에는 세포의 현재 상태가 강하게 유지되는 경향이 있는 반면 Rac1이 활성화 되면 그 주위로 액틴섬유들의 모양이 변화하면서 lamellipodia가 형성이 되고 세포의 모양이 변하게 된다.
카데린 전환이 일어나 세포연접부위가 E-카데린에서 N-카데린으로 바뀌게 되면 Rac1의 분포도 바뀌게 된다. Rac1은 세포연접에 E-카데린이 많이 존재하며 안정적으로 결합이 유지되고 있을 때는 E-카데린 근처에 많이 분포하다가 카데린 전환이 일어나 N-카데린으로 바뀌게 되면 세포연접 부위로부터 멀어지게 된다. Rac1이 연접부위가 없는 다른쪽으로 이동하게 되면 그 부위를 중심으로 액틴에 의한 세포골격이 재형성되게 되고 세포의 무게중심이 세포연접부위에서 다른 곳으로 옮겨지게 된다. 세포 내의 물리적 긴장의 위치가 변하게 되면서 N-카데린에 의해 연결되어있던 세포결합이 붕괴되면서 세포의 이동이 시작된다[23]. Rac1이 E-카데린이 있을 때는 세포연접부위 근처에 있다가 N-카데린으로 바뀌자 반대편으로 이동하게 되는 과정에 대해서는 아직 밝혀지지 않았다.
두경부암에서의 상피-간엽이행
두경부암에서 상피-간엽이행과 관련된 연구들은 다른 암에 비해 활발하게 이루어지고 있지는 않은 상태이며, 조직이나 혈액에서 상피-간엽이행과 연관된 biomarker의 발현을 조사하여 두경부암에서의 상피-간엽이행의 역할을 규명하는 연구가 간간히 있어온 정도이다. 연관되는 biomarker로는 간엽형 세포에서 발현되는 vimentin, N-cadherin, fibronectin과 상피형 세포에서 발현되는 E-cadherin, cytokeratin 등이 있으며, 상피-간엽이행의 전사인자인 Snail, Slug, Twist, ZEB1, ZEB2 등이 있다.
80명의 두경부 환자를 대상으로 한 상피-간엽이행 연구를 보면 N-카데린이 높게 발현한 52명의 환자의 예후가 유의하게 안좋은 것으로 나타났으며, 카데린 전환이 일어난 것으로 판정된 30명의 환자들의 조직을 분석한 결과 세포의 침윤도나 임파선 전이가 유의하게 더 높게 나왔다. 또한 두경부암 세포주에서 카데린 전환이 일어난 세포들의 표현형이 간엽형 세포로 변한 것도 확인하였다[24]. 26명의 두경부암 환자를 대상으로 한 다른 연구에서도 E-카데린이 낮게 검출되고 vimentin이 높게 검출되는 환자들은 그렇지 않은 환자들에 비해 2배 이상 높은 전이율을 보였다[25]. 상피-간엽이행의 전사인자인 Slug 발현이 침샘에서 발생한 선양낭성암의 재발과 전이에도 관련이 있다는 연구도 있으며[26], 특히 Slug는 두경부암세포의 단독이동이 아닌 세포군락의 집단이동에 관여한다고 보고된다[27]. 상피-간엽이행을 일으키는 인자로서 가장 널리 알려져있는 TGFβ1은 두경부암에서도 높게 검출되었으며, 두경부암세포주에서도 TGFβ1가 Slug뿐만 아니라 다양한 경로를 통하여 세포의 표현형을 바꾸고 상피-간엽이행을 일으키는 것을 확인하였다[28,29]. 또한, EGFR과 VEGFR, Wnt 등의 다른 성장인자들도 두경부암세포의 상피-간엽이행에 관여하는 것으로 보고된다[30,31]. 저산소증(hypoxia)도 두경부암의 상피-간엽이행과 관련이 있다. HIF-1α가 여러 독립적인 기전을 통해 저산소증에 의해 유발되는 상피-간엽이행을 조절한다[32,33]. 구인두암의 중요한 인자인 인체유두종바이러스 감염은 상피-간엽이행과 관련이 없는 것으로 보고된다. 296명의 구인두암 환자들을 대상으로 한 연구에서 인체유두종바이러스 감염은 E-카데린과 vimentin의 발현과 큰 연관성이 없었다[34].
결 론
현재까지 상피-간엽이행을 유도하는 인자들에 대한 연구나 상피-간엽이행이 일어난 후의 변화된 세포의 특징들에 대해서는 많은 연구가 되어있지만 상피-간엽이행이 일어나는 과정 자체에 대한 연구, 특히 세포막에서의 카데린 전환 과정에 대한 이해는 여전히 부족하다. 특히 E-카데린과 비슷한 구조이지만 완전히 다른 역할을 하는 N-카데린에 대해서는 연구가 거의 이루어지지 않았다. 상피-간엽이행 중 N-카데린이 세포간연접부위에 발현하게 되면 세포접촉이 붕괴되고 반대쪽으로 세포의 재분극이 일어나게 되는 일련의 과정에 대해서는 아직 자세히 모르는 상태이다. 상피-간엽이행에서 필수적인 카데린 전환의 과정에 대한 이해가 부족한 이유는 살아 있는 세포에서 카데린을 제어하면서 세포막 주변 분자들의 변화를 관찰하것을 실험적으로 구현하기 어렵기 때문이다. 다행히 최근에 나노프로브 시스템을 이용하여 살아있는 세포에서 카데린이나 notch 같은 세포막수용체 단백질들을 조절하면서 세포막 주변의 신호전달 과정을 높은 해상도로 영상화할 수 있는 기술들이 개발되어 이에 대한 연구들이 시작되고 있다[35-38]. 카데린 전환 과정과 그후에 일어나는 세포 내의 변화에 기전이 밝혀진다면 이를 이용한 치료제의 개발이 활발히 이루어 질 것이다.