조직공학적 기도재건의 현재
Tissue-Engineered Tracheal Regeneration: Current Status
Article information
Trans Abstract
Tracheal regeneration is very challenging clinical demand because the trachea is not a simple windpipe, but a multilayered, complex structure. The tissue-engineering technique is widely accepted as promising strategy in tracheal regeneration. For successful regeneration, a substitute for trachea should provide not only appropriate laterally rigidity and longitudinally flexibility for sustaining the luminal shape of the trachea, but also favorable environment for respiratory ciliated epithelium, smooth muscle and blood vessel cells to regenerate. To date, a variety of materials such as polyglycolic acid, poly (lactic-co-glycolic acid), polycarprolactone, nanocomposite polymers and many naturally-derived scaffolds have been investigated. With these investigations, several clinical attempt of tracheal replacement with artificial trachea have been tried, but clinical outcome has not been quite satisfying. This article reviews the regeneration of C-shaped cartilage, respiratory ciliated epithelium and neovascularization of artificial trachea, together with the difficulties, plausible options and future perspectives.
서 론
조직공학 및 재생의학(tissue engineering & regenerative medicine)은 여러 가지 질병, 노화, 사고로 인해 기능을 상실한 장기를 재생시키거나 대체하기 위해 조직 이식물(tissue implant), 나아가 인공장기(artificial organ)를 개발하기 위한 다학제 학문이다[1,2]. 일반적으로 환자 자신에게서 분리, 배양된 특정 세포를 생체적합한(biocompatible) 재료로 구성된 지지체(scaffold)에 생착시키고, 생체활성인자(bioactive factor) 또는 생체반응기(bioreactor)를 이용한 자극(stimulation), 분화(differentiation) 과정을 통해 조직 재생을 유도한다[3]. 즉, 공학적-생물학적 기술을 이용하여 우리 몸의 생체조직과 유사하게 제작된 자가 조직의 대체제 및 인공장기를 이용하여 다양한 임상적 질환을 해결할 수 있는 가능성을 제시하고 있다. 즉, 기존의 수술적 혹은 약물적 치료에 반응하지 않아 기능을 잃은 장기나 손상된 조직을 다양한 공학-생명과학-의학적인 지식을 이용하여 재생시키는 접근방법인 것이다.
선천적 혹은 기타 질환으로 인해 발생한 기관(trachea) 전장의 50% 이상 기관결손(tracheal defect)의 경우 단단문합술(end-to-end anastomosis)로는 재건이 불가능한 것으로 알려져 있다[4,5]. 이러한 기관의 결손은 종양, 기관절개술, 선천성 질환, 기도삽관의 장기화 또는 다양한 종류의 기관손상에 의해서 발생할 수 있으며, 이는 생존에 중요한 발성, 연하, 호흡, 점액섬모 청소능(mucociliary clearance), 호흡 항원에 대한 면역 등 기능의 저하를 일으킬 수 있다[6,7]. 기관은 단순한 원통형 구조가 아니라 내부의 C자 모양의 연골이 존재하며, 호흡 섬모 상피(respiratory ciliated epithelium) 및 연조직으로 구성된 다층구조(multi-layered structure)이다. 일반 연조직에 비해 탄력성이 떨어지고 단단하며, 길이가 길고 주요 심혈관 조직과 접해 있어 치료가 어려운 해부학적 특징이 있고, 일단 손상이 되면 내부의 호흡 섬모 상피와 정상적인 연골이 재생되지 않고 섬유화, 상처조직화에 의해 회복되어 일반적인 치료에는 반응하지 않는 특징이 있다. 따라서 대안적 치료의 개발이 시급한 상태이며, 조직공학적 기관재건(tissue-engineered tracheal regeneration)이 그중 한 방법으로 주목을 받으며 최근까지 여러 기초적, 임상적인 결과를 보여주고 있다. 하지만 몇몇 희망적인 결과에도 불구하고, 조직공학적 기관재건술을 직접 환자에게 적용하기에는 넘어야 할 장애물이 많은 것으로 판단되며, 본 논문에서는 최근까지 진행된 여러 재생의학-조직공학적 기도재건의 연구결과들을 정리하여 앞으로 나아갈 방향에 대해 고찰해 보고자 한다.
조직공학적 기관재건의 필수 요소
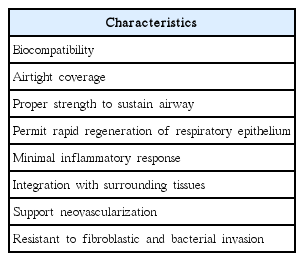
기관을 대체하기 위한 조직의 이상적인 조건은 여러 문헌에서 보고된 바 있으며, 정리하면 Table 1과 같다[8-10]. 이 중 가장 중요한 것은 좌우에서의 압력에도 무너지지 않고 기도(airway)를 유지하는, 측면강직도(lateral rigidity)와 두경부의 움직임에도 파열되지 않는 종적유연성(longitudinal flexibility)으로 대별되는 기계적 특성(mechanical properties)이다[6]. 뿐만 아니라 감염, 육아조직형성을 막고, 가래를 배출할 수 있는 호흡 섬모 상피 재생도 성공적인 기관재생을 위해 반드시 필요한 조건이다. 이외에도 생채적합성, 면역적합성, 혈관재생능, 및 소아 환자의 경우 성장가능성 또한 인공기관 대체물이 해결해야할 필수과제이다.
C-자형 기관 연골재생(C-shaped tracheal cartilage regeneration)
전술하였던 것처럼, 조직공학적 기관재생을 통해 기도(airway)를 유지하기 위해선 신생 인공기관(artificial trachea)의 기계적 강도 및 유연성이 무엇보다도 중요하다. 인체 내에서 이러한 기계적 특성은 C-자형 기관 연골과 주변 연조직의 보강으로 유지되고 있다. 적절한 기계적 특성을 만족시키고 성공적인 기관연골의 재생을 위해 먼저 고려해야 할 것이 지지체의 선택이다.
생체 지지체는 독성이 없으면서, 인체 내 이식 시 혈액 응고나 비정상 염증반응을 유도하지 않는 생체적합성과 대체하려는 각각의 장기에 맞는 적절한 물리적 특성을 가져야 한다. 그러나 현재까지 개발되어 적용되고 있는 소재들은 아직 해결하지 못한 문제점들을 지니고 있다. 전통적으로 천연유래 지지체(naturally-derived scaffold)는 조직공학 및 재생의학영역에서 오랫동안 사용되어 왔다. 천연유래 지지체는 세포 전달 및 침투유도(cell delivery & recruitment), 세포생착(cell attachment), 생체적합성(biocompatibility), 생분해성(biodegradability), 연골재생(chondrogenesis)에서 장점을 갖지만, 기계적 강도는 약하며, 가공성이 떨어져 3차원적인 모양을 제작하는 데 어려움이 있다[11]. 대표적으로 콜라겐(collagen) [12], 피브린과 히알루론산(fibrin/hyaluronic acid) [13,14], 키토산(chitosan) [15], 돼지연골유래 지지체(porcine cartilage powder) [16,17]등이 천연유래 지지체로써 기관재생에 시도되었다. 반면, 합성 지지체(synthetic scaffold)는 천연유래 지지체와 비교하여 우수한 물성 및 가공성에서 장점을 가지며, 모양을 만들거나 조작이 용이하나 낮은 생체적합성과 낮은 조직 재생능력으로 인해 세포생착, 연골재생 및 신생혈관 형성 등에서는 약점을 보인다[18]. 대표적으로 polyglycolic acid(PGA), polylactic acid/PGA, poly(lactic-co-glycolic acid), polyester urethane, Pluronic F-27(Sigma-Aldrich, St. Louis, MO, USA) 등이 시도되었으며, 합성지지체 단독 혹은 천연유래 지지체와 함께 사용되어, 여러 동물 모델에서 어느 정도 성공적인 기관재생능을 보여주고 있다[18-21]. 최근에는 3D 프린터에서 독성유기용매 없이도 사용이 가능한 polycarprolactone이 각광을 받고 있다[22]. 하지만 천연유래 지지체와 합성지지체 모두 여러 가지 면에서 해결해야 할 과제가 남아있는 것이 사실이다. 조직공학적 기관 재생에 사용하기 위한 지지체의 실용화를 위해서는 생체소재의 특성으로 요구되었던 기관의 구조적 골격으로서 역할을 할 수 있는 물성, 세포의 생착과 증식능력 향상, 육아조직 없는 주변조직과의 융화, 그리고 일정기간 이후 분해될 수 있는 생분해성 등이 넘어야 할 장애물이라 하겠다.
조직공학적 기관재생, 연골재생에 있어 지지체 이외에 중요한 요소는 이식세포의 선택이다. 성공적인 연골재생을 위해서 선택할 수 있는 세포에는 연골세포(chondrocytes)와 여러 종류의 줄기세포(stem cells)가 있다. 가장 먼저, 연골세포는 Vacanti등[23]이 보고한 최초의 조직공학적 기관재생 연구에서도 사용되었으며, 이후에도 C-자형 기관 연골재생을 위해 많은 연구에서 사용되고 있다[14,16,19]. 역분화(de-differentiation)의 문제점이 있기는 하지만 연골세포 배양, 증식 및 재생 연골의 체외(in vitro) 생성은 잘 확립되어 있는 접근방법이다[24]. 면역반응을 고려하여 자가(autologous) 혹은 동종(allogenic) 연골 세포를 사용할 것인지, 연골의 공여부로 선택이 가능한 기관, 비중격 혹은 이개연골 등 중에서 어느 곳을 선택할지는 아직 연구자에 따라 여러 의견이 있는 상태이다.
한 가지 세포공급을 통해 여러 조직을 동시에 재생하기 위한 가장 이상적인 세포 종류인 줄기세포(stem cells) 또한 기관 재생을 위한 연구에 사용되어 왔다. 잘 알려져 있는 것처럼 줄기세포는, 배아조직에서 얻어지거나 성인의 경우 특정 부위에 소량 존재하는 특별한 세포로서, 형질의 변화 없이 무한 증식이 가능하고(self-renewal), 연골, 혈관, 신경, 근육 등 다양한 종류의 조직으로 분화(multipotent differentiation)할 수 있음이 잘 알려져 있다. 이러한 줄기세포는 재생의료의 핵심 요소로서 전 세계적으로 활발하게 연구가 진행되어 왔다. 줄기세포 중 배아줄기세포(embryonic stem cells)의 경우 적절한 자극에 의해 거의 모든 종류의 세포 형태로 분화할 수 있으나 윤리적 문제와 기형종(teratoma) 형성 등의 가능성으로 실제 사용이 제한적이다. 성체 줄기세포(adult stem cells)는 모든 종류의 세포로 분화하지 못한다는 단점이 있지만, 배아줄기세포에 비해 윤리적인 논란에서 비교적 자유로운 이점을 가져, 재생의학에서 많이 연구되어 왔다. 성체 줄기세포는 다양한 조직에서 발견되며, 골수(bone marrow), 피부의 기저층, 소장(small intestine)의 내막, 뇌 등에서 얻을 수 있다. 이 중 근육, 연골, 골 등 중간엽 조직 및 신경, 피부로 분화되는 중간엽 줄기세포(mesenchymal stem cells, MSCs), 특히 골수 유래(bone marrow-derived), 지방유래(adipose-derived) 중간엽 줄기세포가 기관재생 연구에 많이 사용되어 왔다[17,25,26]. 중간엽 줄기세포는 특별한 부작용 없이 연골세포와 유사하게 성공적인 연골재생을 유도하는 것으로 알려져 있다. 줄기세포 연구가 발전함에 따라서 유도만능 줄기세포(induced pluripotent stem cells) 또한 기관재생 연구에 시도되고 있다[27,28]. 유도만능 줄기세포란, 최종적으로 분화가 완료된 세포가 만능분화능력(pluripotency)을 가지도록 인위적인 역분화 과정을 거쳐 유도된 세포들을 말하며, 최근 많은 연구가 진행 중이다. 하지만 기관재생에의 적용, 나아가 재생의학에의 임상적 적용에는 아직 더 많은 연구가 필요한 상태이다.
호흡 섬모 상피 재생(Ciliated respiratory epithelium)
정상적인 기관에서 기관의 내면은 점액 분비 및 청소에 중요한 기능을 갖는, 섬모를 포함하고 있는 가성증층원주 상피(pseudostratified columnar epithelium)로 덮여 있다[29,30]. 호흡상피는 섬모 상피세포(ciliated columnar cells), 배상세포(goblet cells), 및 기저세포(basal cells) 등 다양한 기능을 가지는 세포로 구성되어 있다[6]. 모든 세포들은 기저막에 닿아 있으며, 일부 분만 강 내(luminal surface)에 접촉되어 있다. 배상세포는 점액(mucus)을 호흡상피 위로 분비하여 외부 세균 혹은 입자들을 제거하며, 더 나아가 감염, 염증 등에 대한 면역반응을 담당한다. 섬모세포의 경우, 여러 개의 운동성을 갖는 섬모가 첨단(apical side)에 존재하여 정돈된 움직임(coordinated movement)을 만들어 낸다. 이러한 움직임은 점액섬모 청소기능(mucociliary clearance)에 중요한 역할을 한다. 기저세포는 기저막에 존재하고, 기도와는 접촉하지 않으며, 줄기세포와 비슷한 특성을 보인다. 이러한 다층구조의 호흡 점막을 성공적으로 재생시키지 못할 경우, 육아조직이 발생하며, 감염 및 점액의 정체가 발생하여 치명적인 기도의 폐색이 발생하게 된다.
다양한 조직 유래 기관지 상피세포(airway epithelial cells)를 이용한 호흡 섬모 상피 재생이 시도되었다. 가장 많이 이용되었던 원천(source)은 비갑개(turbinate) 혹은 비중격(nasal septum) 유래 호흡 섬모 상피이다. 공기-액체 계면 방식(air-liquid interface technique)의 배양방법을 통해, 비강조직 유래세포에서 성공적으로 다층의 호흡상피를 배양할 수 있음이 입증되었다[6,31]. 이외에도 협부점막(buccal mucosa), 심지어는 피부 상피세포에서도 기도상피를 분화시키는 연구 보고가 있어 왔으나[32,33] 분화 과정이 매우 복잡하고 어려우며, 충분한 세포를 증식시키는 것은 거의 불가능하여 추가적인 개선이 반드시 필요한 상태이다.
이렇게 호흡상피는 충분한 양을 채취하기가 쉽지 않으며, 실험실 환경에서 배양하여 증식하는 것이 쉽지 않아, 배아줄기세포를 이용한 호흡 섬모 상피 분화 연구도 활발히 진행되어 왔다. Coraux 등[34]은 배아줄기세포에서 섬모 상피, 기저세포(basal cell), 배상세포(goblet cell) 등을 포함한 호흡상피를 분화시키는 데 성공했다. 유사하게 만능유도 줄기세포에서 호흡상피가 분화 가능함이 보고된 바 있다[27]. 내배엽 기원인 호흡상피를 외배엽 혹은 중배엽 기원 조직이나 세포로부터 분화시키는 시도는 성공률이 높지는 않은 상태이다. 같은 이유로 중간엽 줄기세포(MSCs) 기원 호흡상피 분화도 몇몇 보고를 제외하고는 아직까지는 성공적이지 못하다.
조직공학적 기관의 인체 이식(Transplantation of Tissue-Engineered Trachea)
조직공학적 기관의 인체 이식은 몇몇 시도가 있어 왔지만, 부분 결손의 재건이거나, 높은 합병증 발생률 및 치명률로 인해 아직 안정적이며 성공적인 임상 결과를 보고한 방법은 개발되지 않은 것이 현실이다. Omori 등[35]이 2005년 탈장수술 이나 흉벽재건에 사용되던 합성지지체인 Marlex(polypropylene; Ethicon Inc., Somerville, NJ, USA)로 구성된 튜브를 콜라겐(collagen)으로 코팅하고, 안쪽에 나선형 링(재질; polypropylene)을 보강하여 기관이식물을 제작하였고, 이를 이용해서 갑상선 기관침범으로 인한 부분 기관결손(partial tracheal defect)을 성공적으로 재건한 것이 조직공학적 기관 인체 이식의 첫 성공 보고이다[36]. 이후 2008년 Macchiarini 등[25]이 결핵에 의한 난치성 기도 협착질환을 가진 30세 여성 환자에서 사체(cadaver)에서 획득한 약 7 cm의 기관을 탈세포과정(decellularization)을 거치고, 수혜자 호흡상피세포 및 연골세포를 생물반응장치(bioreactor)를 이용 및 이식하여 성공적인 결과를 보고하였다[37]. 이후 몇몇 연구자들이 세포제거방법의 개선이나 주변조직 보강방법의 도입 등 이식방법의 개선을 통한 사체 유래 탈세포 기관(cadaver-derived decellularized trachea)이식 보고가 몇 차례 있었다[38,39]. Macchiarini 등[25]은 추가로 합성 nanocomposite [polyhedral oligomeric silsesquioxane poly(carbonateurea)urethane]와 환자 세포(autologous bone marrow mononuclear cells), 생물반응장치를 이용한 조직공학적 기관재건 사례를 보고하여 성공적인 결과를 보여주는 듯 하였다[40]. 하지만, 최근 연구윤리 위반(scientific misconduct)에 대한 대대적인 조사가 있었고, 의혹이 사실로 판명되어 학계를 큰 충격에 빠뜨렸다[41-44]. 조사결과에 따르면 2011~2014년까지 합성지지체를 이용한 기관이식수술을 받은 9명의 환자 중 7명이 사망하고, 한 명은 이식된 기관을 제거한 것으로 밝혀졌다. 따라서 조직공학적 기도재건, 특히 원통형 결손의 경우는 인체 적용에 좀 더 연구가 필요할 것으로 생각된다.
결 론
재생의학-조직공학은 인체 내에 질병과 노화 및 사고로 인해 손상된 조직을 적절한 조작을 통하여 재생시키거나, 외부에서 인공적으로 만들어진 이식물을 이용하여 정상조직과 융화(integration)시켜 조직 고유의 해부학적, 생리학적인 기능을 재현시킬 수 있는 종합적인 시도를 포함하고 있다. 의학, 생명과학 이외에도 화학공학, 재료공학 등의 융합학문으로 시작된 조직공학 및 재생의학은 그 태동으로부터 약 30여 년을 넘지 않는 짧은 역사에도 불구하고 최근 많은 연구가 집중되고 있으며, 더불어 다양한 연구배경을 가지고 있는 연구자들의 학제 간 연구가 활발히 진행되고 있다. 적극적인 연구의 결과로 개발된 새로운 조직공학적 기술들에 대한 다양한 임상시험이 진행 중이며, 가까운 미래에는 실제 임상의학에 사용될 수 있기를 기대하고 있다.
20세기에 들어서 기도재건에 대하여 재생의학-조직공학적 관점에서 활발한 연구가 이루어지고 있다. 그렇지만 기관의 기능과 구조, 이를 재생시키는 기술에 대한 연구가 깊어질수록 기도재건이 단순한 도관(tube, windpipe) 재건이 아니며, 더 복잡하고 어려운 것임을 알 수 있다. 대표적으로 거부반응 및 염증반응을 최소화하는 점, 기도(airway)를 유지할 만한 물리적인 강도를 유지하는 점, 호흡상피를 적절하게 재생시키는 점, 이식물에 신생혈관 형성이 잘 되도록 하는 점, 그리고 육아조직의 생성 및 재협착을 방지해야 하는 점 등에 대한 문제를 우선적으로 해결해야 할 것이다. 이러한 과제들을 하나씩 해결해 나간다면, 해부학적, 생리학적 특성을 온전하게 가진 신생 기관의 제작 및 환자에의 적용이 요원하지 만은 않을 것이다.
Acknowledgements
This research was supported by a grant from the Korea Health Technology R&D Project through the Korea Health Industry Development Institute, funded by the Ministry of Health & Welfare, Republic of Korea (grant number: HI14C2108).